来源:智慧医械,未经授权不得转载
小肠长度超过20英尺,但宽度只有一英寸。常规软式内镜难以抵达5-7米的小肠,造成小肠疾病难以被发现,曾被认为是胃肠镜检查中的“黑暗大陆”。小肠出血也曾经被称为“不明原因消化道出血”。
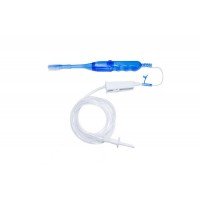
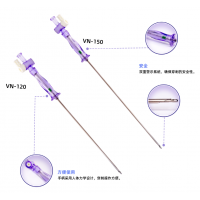
小肠镜是诊断和治疗小肠病变的重要手段,而气囊内镜检查已经成为诊断和治疗小肠疾病的标准方法之一,可分为双气囊电子小肠镜(DBE)、单气囊电子小肠镜(SBE)。简单来说,双气囊小肠镜就是在长200cm的镜子外装一个带气囊的外套管(长145cm),同时在小肠镜头端安装一个气囊;而单气囊小肠镜则镜子头端没有气囊。两者操作性能有所不同,但都可用于小肠检查及治疗。
气囊通常是表面光滑的球形,防止肠道粘膜损伤所需的压力限制降低了气囊锚定力。因此,气囊在进行内镜检查时容易滑落,不易在肠道中某一位置固定进行深入检查,尤其是在进行组织切割操作过程中。这些问题导致程序不完整或时间延长,每年因为内窥镜检查失败造成的医疗花费高达1亿美元。
Aspero Medical是一家专注于球囊内镜通路的美国医疗器械企业,创立于2018年,得到了Innosphere Ventures的初始股权资金支持。该公司开发的Ancora-SB小肠球囊外套管采用专利Pillar微纹理球囊技术,对球囊表面纹路进行处理,可最大限度地提高摩擦性能,改善胃肠道粘膜壁牵引力和固定的稳定性。
Aspero Medical公司的Pillar™气囊与普通乳胶气囊(有润滑和无润滑)在锚定力上的对比。未润滑的Aspero Medical Pillar™气囊的锚定力高于未润滑的乳胶气囊,但差距较小。在润滑后,Pillar™气囊的锚定力相比乳胶气囊显著提高了80%。
2024年初,Aspero Medical获得了美国国立卫生研究院(NIH)190万美元的SBIR第2期资助,用于完成一项名为“Ancora-SB气囊套管在内镜检查中的完全定位和光学可视化”的双盲的、多中心的随机对照试验(RCT)。

该研究旨在证明Ancora-SB气囊套管优于现有护理标准,并评估其扩大使用指征的潜力。研究将专注于小肠中段的气囊内镜检查,预计于2024年底完成。今年初,该研究的第一位患者已经入组。圣路易斯华盛顿大学医学院内镜介入科主任兼医学教授Vladimir Kushnir博士表示:“我们非常高兴第一位患者入组了NIH资助的随机对照试验。这标志着我们迈出了展示Ancora-SB气囊套管作为诊断和治疗小肠疾病的可靠平台的第一步,”
其实,Ancora-SB在2023年就通过了FDA许可(510K),用于小肠内出血治疗。而用于大肠内组织切除的Ancora-LB预计将于2024年底通过FDA许可。用于胃/食管内组织切除的Ancora-GE预计将于2025年底通过FDA许可。
Aspero的首席医疗官Steven Edmundowicz博士表示:“越来越多的小肠疾病患者要求我们开发创新的诊断和治疗方案。例如说Ancora-SB这样的设备,能够提高小肠镜检查程序的效率。我们希望Ancora-SB在需要创新设计的情况下可以得到应用。”
Innosphere Ventures Fund的合伙人Mike Freeman表示:“目前用于胃肠内镜检查的技术存在显著的局限性,但Aspero开发了一种可能改善某些程序性能的替代方案,节省医务人员和患者的时间,并改善患者的结果,我们期待继续支持公司及其持续的产品开发工作。”

 安科高技术
安科高技术 医准智能
医准智能 明峰医疗
明峰医疗 迈瑞医疗
迈瑞医疗 之江生物
之江生物 雷杜生命
雷杜生命 迪瑞医疗
迪瑞医疗 万泰生物
万泰生物 迈克生物
迈克生物 爱威科技
爱威科技 基蛋生物
基蛋生物 万孚生物
万孚生物 睿心医疗
睿心医疗 润迈德医疗
润迈德医疗 爱博医疗
爱博医疗 佗道医疗
佗道医疗 瑞龙诺赋
瑞龙诺赋 微光医疗
微光医疗 联影医疗
联影医疗 内镜精灵
内镜精灵 精微视达
精微视达 迈瑞医疗
迈瑞医疗 迪安诊断
迪安诊断 华科精准
华科精准 威高机器人
威高机器人 精锋医疗
精锋医疗 微创机器人
微创机器人 术锐技术
术锐技术 业聚医疗
业聚医疗 佰仁医疗
佰仁医疗 博迈医疗
博迈医疗 健世科技
健世科技 启明医疗
启明医疗 赛诺医疗
赛诺医疗 沛嘉医疗
沛嘉医疗 先健科技
先健科技 美国DVI订制式医用放大镜、LED手术照明灯
美国DVI订制式医用放大镜、LED手术照明灯 麦迪特多参数监护仪MD908B心电监护
麦迪特多参数监护仪MD908B心电监护 健康一体机HS-V300
健康一体机HS-V300 柯尔压缩雾化器WHC
柯尔压缩雾化器WHC 无纺布空白帖膏药空白帖医用透气胶带贴三伏贴空白帖PU膜空白贴
无纺布空白帖膏药空白帖医用透气胶带贴三伏贴空白帖PU膜空白贴 Drager新生儿ISO直型流量传感器接头8411130
Drager新生儿ISO直型流量传感器接头8411130 除颤仪心脏除颤器电极片儿童AED Pad
除颤仪心脏除颤器电极片儿童AED Pad 制氧机出租柯尔制氧机5升医用氧浓度超静音制氧机出租
制氧机出租柯尔制氧机5升医用氧浓度超静音制氧机出租